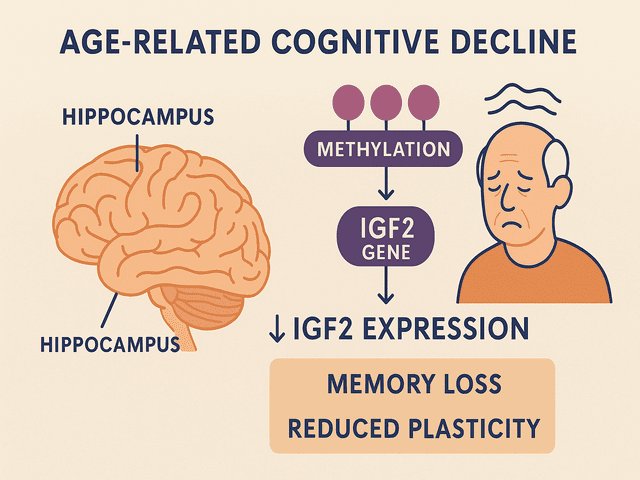
La investigación revela que el gen IGF2, clave para la formación de recuerdos, sufre un aumento de metilación (una marca epigenética que reduce su expresión) en el hipocampo de individuos envejecidos, lo que impacta directamente en su capacidad para aprender y recordar.
El estudio publicado bajo el DOI 10.1016/j.brainresbull.2025.111509 identifica cómo la metilación del gen IGF2 en el hipocampo regula el deterioro cognitivo asociado al envejecimiento.
Mecanismos biológicos del deterioro cognitivo asociado al envejecimiento
El papel del gen IGF2 y su regulación epigenética
El gen IGF2 (factor de crecimiento similar a la insulina 2) está ampliamente implicado en la plasticidad sináptica —es decir, la capacidad del cerebro para adaptarse, aprender y consolidar recuerdos—. En el estudio, se comprobó que en cerebros envejecidos (modelos animales de mayor edad) se observa una mayor metilación del promotor de IGF2, lo que reduce su expresión y afecta la función de las conexiones neuronales. Los autores concluyen que esta alteración epigenética es un factor que regula la pérdida de memoria y la disminución de la plasticidad en la vejez.
Consecuencias funcionales y clínicas
La disminución de IGF2 con la edad puede traducirse en menor capacidad para generar nuevas conexiones entre neuronas, consolidar recuerdos y adaptarse a nuevos estímulos cognitivos. En términos prácticos, esto se manifiesta como olvidos frecuentes, dificultad para aprender nuevas tareas o menor agilidad mental. Este hallazgo aporta una base molecular para el «deterioro cognitivo leve» asociado al envejecimiento, incluso antes de que aparezca una demencia.
Implicaciones para la atención sanitaria y preventiva
Estrategias no farmacológicas con fundamento biológico
Comprender que existe un mecanismo concreto —metilación de IGF2— abre la puerta a intervenciones relacionadas con la estimulación cognitiva, el ejercicio, la alimentación y el sueño, que pueden mantener activa la plasticidad neuronal. Desde la atención a personas mayores, es clave promover programas que potencien la salud cerebral antes de que los daños se vuelvan irreversibles.
Necesidad de detección temprana y seguimiento
Para que los efectos de estas alteraciones moleculares tengan menos impacto, es esencial detectar signos iniciales de deterioro cognitivo, como olvidos leves o cambios en la concentración. Con una intervención temprana basada en estimulación cognitiva y hábitos saludables, se pueden mitigar los efectos de la metilación de IGF2 y preservar la función cerebral durante más tiempo.
Tabla resumen de hallazgos y aplicaciones para envejecimiento cognitivo
| Aspecto observado | Región implicada | Cambio identificado | Aplicación para personas mayores |
|---|---|---|---|
| Aumento de metilación del gen IGF2 | Hipocampo | Menor expresión de IGF2 con la edad | Promoción de hábitos que favorecen plasticidad |
| Disminución de la plasticidad sináptica | Hipocampo | Reducción en la capacidad de formación de recuerdos | Programas de estimulación cognitiva precoz |
| Impacto en memoria y aprendizaje | Hipocampo | Deterioro funcional observado en modelos animales | Evaluaciones cognitivas regulares para intervención |
| Base molecular del deterioro cognitivo | Cerebro envejecido | Evidencia de mecanismo epigenético de declive | Integración con políticas de envejecimiento activo |
Desafíos, perspectivas y recomendaciones
Limitaciones del estudio y pasos siguientes
El trabajo está realizado en modelos animales, lo que limita su traducción inmediata al ser humano. No obstante, marca una dirección clara para futuras investigaciones clínicas. Habrá que confirmar si los mismos cambios epigenéticos se observan en humanos y si es posible revertirlos o mitigarlos.
Integración en la práctica de cuidados a personas mayores
Desde la atención sanitaria y social, es importante que los servicios para personas mayores incluyan valoración regular de la función cognitiva, estimulación estructurada (grupos, talleres, ejercicio físico) y apoyo al entorno que valiéndose de este conocimiento potencie la autonomía y la salud cerebral.
Comunicación y educación sobre envejecimiento saludable
Es esencial trasladar este tipo de hallazgos a un lenguaje accesible para personas mayores, cuidadores y profesionales de atención. Entender que el desgaste cognitivo no es un “destino inevitable” puede motivar a adoptar estilos de vida que favorezcan la plasticidad cerebral y retrasen el declive.
Resumen
El estudio identificado por el DOI 10.1016/j.brainresbull.2025.111509 aporta una base molecular novedosa al entendimiento del deterioro cognitivo asociado al envejecimiento. Al vincular un aumento en la metilación del gen IGF2 con la pérdida de memoria y deterioro de la plasticidad en el hipocampo de cerebros envejecidos, abre la puerta a nuevas estrategias preventivas centradas en mantener la función neuronal. Para las personas mayores, los cuidadores y los profesionales del envejecimiento saludable, este hallazgo refuerza la importancia de la detección precoz, la estimulación cognitiva y los entornos que favorecen la autonomía mental. Cuidar el cerebro es tan importante como cuidar el cuerpo para una vida más larga y de mayor calidad.
Referencias
https://www.sciencedirect.com/science/article/pii/S0361923025003211
Más info sobre la ONG Guía de Mayores en su blog
![]()